Pomôžte rozvoju stránky a zdieľajte článok s priateľmi!
Čo je vnútri? Túto otázku si položil každý. Toto je jedna z vlastností prirodzenej ľudskej zvedavosti.
Túto zvedavosť uspokojujeme už od detstva. Čím dlhšie si dokážeme klásť túto otázku (a ostatným podobným), najlepšie až do vysokého veku, tým bohatší bude náš život.
Ale čo sa vlastne pýtame? Dieťa pri pohľade do vnútra hračky najskôr hľadá nejakú novú štruktúru materiálu. Mladý muž, ktorý sa pozerá do knihy alebo internetu, hľadá predovšetkým informácie – menej ho zaujíma, z čoho sú vyrobené.Archeológ, ktorý skúma novovykopanú historickú budovu, hľadá informácie aj materiálnu štruktúru – tá sa tiež premení na informáciu. Tak isto geológ hľadiaci (kladivom a dlátom, lupou, röntgenom) do hlbín horniny hľadá tam minerály a symetriu a krásu.
Je potrebné zmeniť vonkajšiu štruktúru alebo dokonca zničiť to, čo chceme vidieť vo vnútri? Našťastie nie! Do vnútra ľudského tela sa totiž lekár pozerá pomocou celého arzenálu nástrojov a nástrojov. Modernú medicínu si ceníme pre jej minimálne invazívny alebo takmer neinvazívny prienik. Nie je potrebné pozerať sa dovnútra pomocou ľudských zmyslov - môžeme vidieť pomocou ultrazvuku, röntgenu, rádiových vĺn a mnohých ďalších metód.
Sme vždy pripravení na to, že sa musíme pozrieť dovnútra? Samozrejme, že nie, zvážte napríklad pohľad do zatuchnutého vajíčka. Alchymisti často zvažovali ich zmesi s ohňom - niekedy explodoval, pretože vo vnútri bola okrem štruktúry a informácií uložená aj energia.Pohľad do vnútra atómového jadra dokonca umožnil predpovedať, aj keď nie okamžite, že „bude z toho energia.“
Teória - stručná a jasná
Na konci prvého desaťročia 20. storočia sa Ernst Rutherford spolu so svojimi kolegami Hansom Geigerom a Ernestom Marsdenom pozrel do vnútra atómu. Objekt, ktorého existencia o storočie skôr nebola ničím iným ako hypotézou, zvedavosťou zdedenou od Demokrita a niektorých iných starovekých mysliteľov. Objekt, o ktorom sa ešte v polovici 19. storočia považovalo, že vo vnútri nič nemá. Objekt, ktorý sa nakoniec stal tak malým, že ho nebolo možné vidieť – vedelo sa len to, že existujú skôr atómy. Ako vyzerali vo vnútri atómu? Čo hľadali? čo videli? Bolo to to, čo očakávali, alebo niečo úplne iné? Určite stojí za to si o tom všetkom prečítať
 Ryža. 1. (Zľava doprava) Ernest Rutherford, Hans Geiger a Ernest Marsden navrhli a uskutočnili sériu experimentov v rokoch 1908 až 1911, v ktorých študovali distribúciu hmoty v atóme. Po interpretácii výsledkov vyvinuli planetárny model atómu.
Ryža. 1. (Zľava doprava) Ernest Rutherford, Hans Geiger a Ernest Marsden navrhli a uskutočnili sériu experimentov v rokoch 1908 až 1911, v ktorých študovali distribúciu hmoty v atóme. Po interpretácii výsledkov vyvinuli planetárny model atómu.
Devätnáste storočie prinieslo množstvo vedeckého výskumu na hranici medzi chémiou a fyzikou. To zahŕňalo výskum problému „prvok verzus zlúčenina“, kvantitatívneho aspektu chemických reakcií vrátane fenoménu elektrolýzy, ako aj v oblasti termodynamiky a optiky. Objavil sa koncept Avogadroho čísla.
Objasnenie správania sa látky v prchavom stave bolo veľkým úspechom kineticko-molekulárnej teórie. Predpokladala zrnitú štruktúru hmoty, teda existenciu najmenších častíc hmoty: atómov alebo ich presne definovaných skupín – molekúl. Toto je najčastejšie uvádzaný príklad; na základe podobných predpokladov sa vysvetľuje aj mnoho ďalších javov. Štúdie hmoty v pevnom stave zase umožnili odhadnúť veľkosť jednotlivých atómov (obr. 2).
Ukázalo sa, že bez ohľadu na prvok boli tieto rozmery rádovo jeden alebo dva angstromy. Podarilo sa nám odhadnúť aj hmotnosti rôznych atómov – ukázalo sa, že súvisia s hmotnostným číslom A prvku. Atómy boli známe ako elektricky neutrálne.
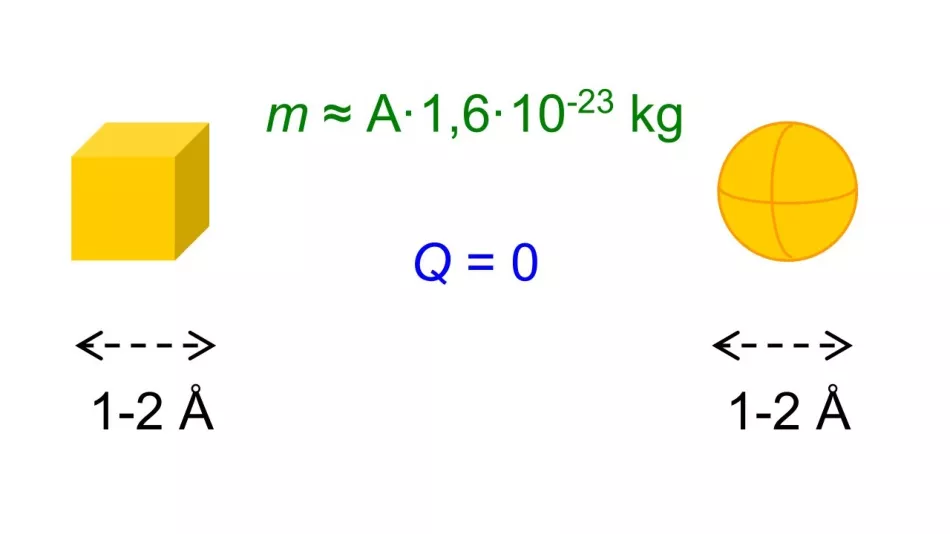 Ryža. 2. Či už boli atómy znázornené ako gule, kocky alebo iné tvary, boli známe ich približné rozmery, atómové číslo Z a hmotnostné číslo A a bola známa aj ich elektrická zotrvačnosť.
Ryža. 2. Či už boli atómy znázornené ako gule, kocky alebo iné tvary, boli známe ich približné rozmery, atómové číslo Z a hmotnostné číslo A a bola známa aj ich elektrická zotrvačnosť.
Čo je vo vnútri atómu?
Nečakaným výsledkom tohto výskumu bol objav vnútornej štruktúry atómov. Katódové lúče, známe už niekoľko desaťročí, boli v prvej dekáde 20. storočia rozpoznané ako zväzky „atómov elektriny“ (dnes poznáme: elektróny) s vlastnosťami nezávislými od materiálu, z ktorého sú emitované. Záver môže byť len jeden: elektróny sú súčasťou každého atómu. Ich nenulový elektrický náboj (dnes poznáme záporný), ako aj ich vtedy známa hmotnosť (o tri až štyri rády menšia ako hmotnosť atómu) však naznačovali, že atómy ešte musia mať nejaké zložky (obr. 3).
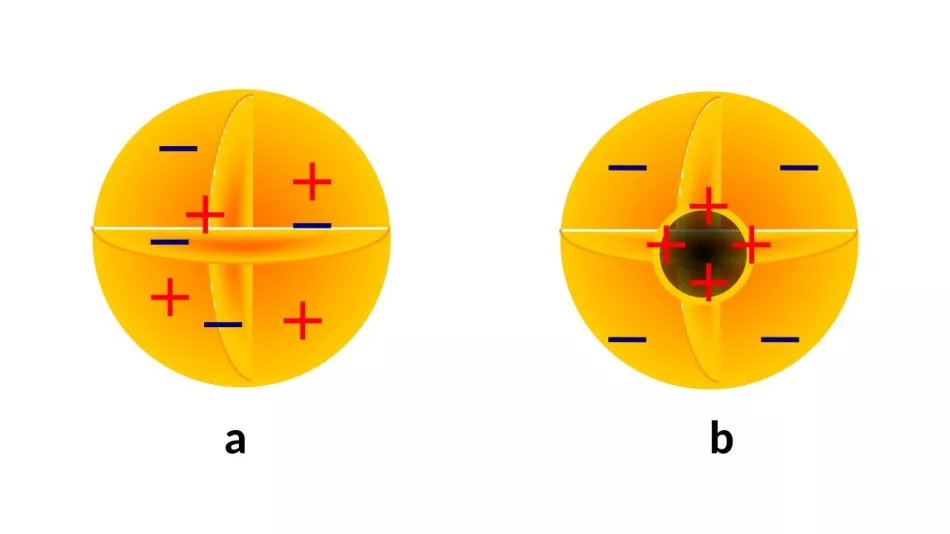 Na prelome 20. storočia bolo vyvinutých niekoľko modelov na opis priestorového rozloženia hmoty a náboja. Niektorí (obr. 2a) predpovedali rovnomerné rozloženie hmoty a náboja vo vnútri atómu.
Na prelome 20. storočia bolo vyvinutých niekoľko modelov na opis priestorového rozloženia hmoty a náboja. Niektorí (obr. 2a) predpovedali rovnomerné rozloženie hmoty a náboja vo vnútri atómu.Prevládal však názor existencia jadra atómu (obr. 2b) - kladne nabitá, masívna vnútorná podštruktúra, s ktoré elektróny sú spojené tak či onak, nemusia byť nevyhnutne symetrické.
Problém bol o tom, ako sú zložky usporiadané vo vnútri atómu, vrátane povahy ich možného pohybu. Boli predložené rôzne hypotézy, hoci prevládal názor, že:
- hmotnosť atómu súvisí s tým, čo je v ňom kladne nabité (Rutherford to nazval atómové jadro);
- táto hmota je viac-menej rovnomerne rozložená v oblasti, ktorej veľkosť je menšia ako veľkosť atómu o rádovo, možno dve, t.j. od 0,01Å do 0,1Å;
- V atóme nesmie byť žiadny prázdny priestor, inak sa atómová hmota nebráni pohybu - elektrónový lúč, podobne ako röntgenový lúč, voľne prechádza pomerne tenkými oblasťami hmoty, napríklad cez kovové fólie a hrúbka niekoľko mikrónov.
Ako sa pozrieť do vnútra atómu?
Každý dnešný fyzik vám povie, že je to jednoduché. Všetko, čo je potrebné, je nasmerovať vhodné častice na atóm, ktoré pôsobia ako náboje, a študovať účinky interakcie týchto nábojov so zložkami atómu. Aby sa predišlo účinku interakcie s elektrónmi, náboje musia mať oveľa väčšiu hmotnosť ako hmotnosť elektrónov. Ale tiež musia mať hmotnosť menšiu ako hmotnosť toho, čo chceme študovať v atóme.
Aby sa predišlo nestabilnému výsledku, náboje musia mať tiež dostatočne vysokú energiu. V časoch Rutherforda neexistovali žiadne urýchľovače, takže výber nábojov bol malý: častice α, ktoré objavil pred desiatimi rokmi, celkom dobre vyhovovali týmto podmienkam. Cieľ (fyzici niekedy používajú termín „screen“) pre α-častice boli atómy zlata v tenkej fólii. Rutherford a jeho kolegovia študovali iné kovy, ale zlato, kujný a ťažný kov, umožnilo vytvorenie filmu s hrúbkou až pol mikrometra (0,510-6 m).
Nameraným účinkom interakcie s atómom zlata bol uhol rozptylu častíc α (obr. 3.).
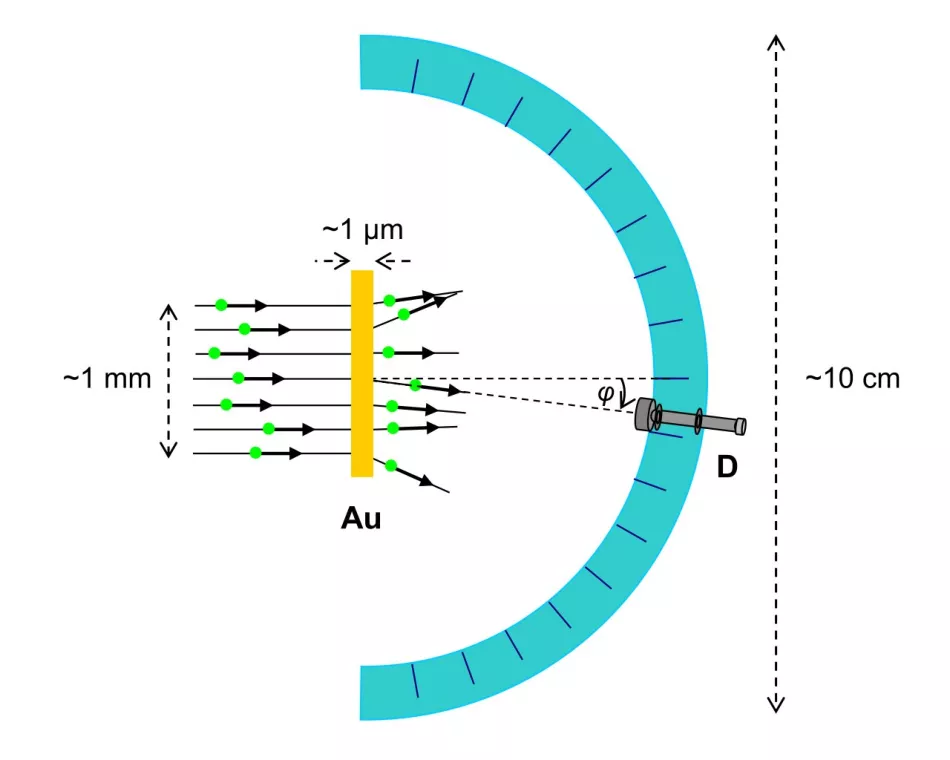 Ryža. 3. Schéma Rutherfordovho experimentu (pohľad zhora)
Ryža. 3. Schéma Rutherfordovho experimentu (pohľad zhora)
α-častice prichádzajú vo forme lúča širokého asi milimeter a sú rozptýlené v kovovej fólii hrubej asi mikrón. Detektor α-častíc je umiestnený v sérii, v rôznych uhloch k počiatočnému smeru lúča, na polkruhovom vodiči s veľkosťou asi decimeter.
Experimentátor sa pozrie do okuláru a spočíta počet zábleskov spôsobených časticami α rozptýlenými pod daným uhlom v určenom čase. Referenčný čas je rovnaký pre všetky uhly.
Uhol rozptylu závisí od viacerých faktorov:
- pre kinetickú energiu Ek častice α,
- nabitý, qa=+2e,
- na náboji jadra (zlato alebo akýkoľvek iný prvok použitý v experimente), t.j. z atómového čísla Z tohto prvku: Q=+Ze,
- z odhadovaného polomeru atómového jadra Rj,
- o parametri dopadu b častice α s jadrom.
Čo sa očakávalo?
Rutherford et al študovali, ako často dochádza k rozptylu pod určitým uhlom φ k pôvodnému smeru letu. V súlade s vtedajšími predstavami o veľkosti atómového jadra očakávali, že tieto uhly budú v obmedzenom, relatívne malom rozsahu. Maximálna hodnota φmuhla rozptylu závisí od odhadovaného polomeru rja je dosiahnutá pre každú z jeho hodnôt pri rôznych hodnotách parametra vplyvu bmObrázok 4 ukazuje dráhu 1 MeV alfa častice rozptýlenej pod maximálnym uhlom za predpokladu, že Rj=0,01 Å. Stalo sa, že α-častica potom prejde cez malú vrstvu jadra.
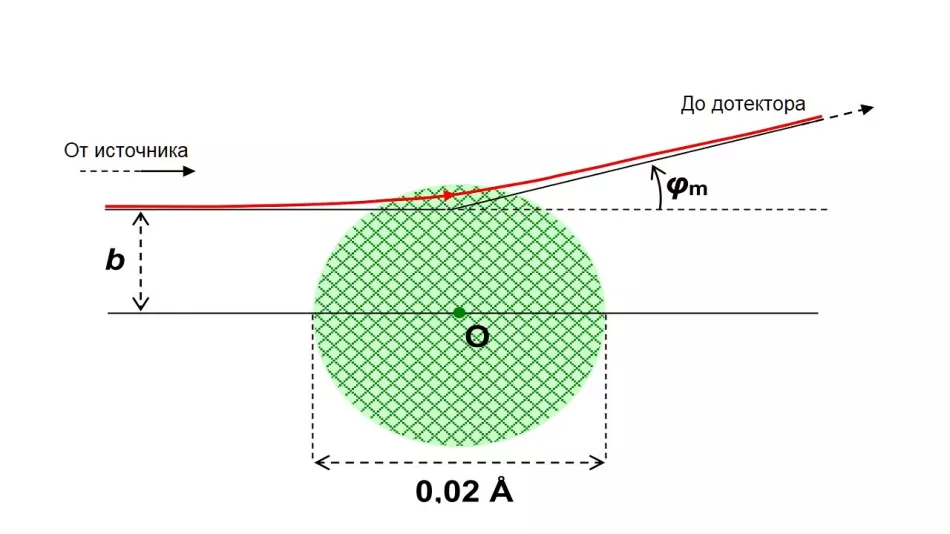 Ryža. 4. Stopa α-častice s Ек=1 MeV, rozptýlená pri interakcii s jadrom atómu zlata.
Ryža. 4. Stopa α-častice s Ек=1 MeV, rozptýlená pri interakcii s jadrom atómu zlata.
Bol prijatý hypotetický jadrový polomer Rj=0,01 Å (10-12 m). To je o viac ako dva rády väčšie ako skutočný polomer jadra atómu zlata. Na tomto obrázku bude menšia ako bodka, ktorá označuje stred atómu.
Parameter zameriavania b ≈ 8-10-13m poskytuje maximálny uhol rozptylu φm ≈ 15°
α častice padajúce s parametrami väčšími ako bma obchádzajúce hypotetické jadro sa vždy rozptýlia pod menším uhlom - letia ďalej od stredu kladného náboja a menej sa odchyľujú. To isté platí pre častice padajúce bližšie k centrálnemu smeru (b
Výsledky výpočtu uhlov φmpre niekoľko hodnôt polomeru atómového jadra, vykonané v súlade s poznatkami o štruktúre atómu zo začiatku 20. storočia sú uvedené v tabuľke 1.Stojí za to pripomenúť, že hodnoty Rj hodnoty menšie ako 0,01 Å pre atómové jadro sa vtedy nebrali do úvahy.
| Polomer atómového jadra Rj | Maximálny uhol lúča φm | Maximálny uhol s parametrom mierenia |
| 0,1 Å | 1,4° | 0,09 Å |
| 0,05 Å | 2,7° | 0,046 Å |
| 0,01 Å | 15° | 0,008 Å |
| 0,005 Å | 37° | 0,003 Å |
Záver: znalosť času nám umožnila získať maximálne uhly rozptylu niekoľko stupňov.
Kognitívny šok experimentátora
Podľa očakávania sa ukázalo, že veľká väčšina α-častíc je rozptýlená pod malými uhlami, rádovo niekoľko stupňov. Ukázalo sa tiež – úplne v rozpore s očakávaniami – že v niektorých prípadoch boli α-častice rozptýlené pod uhlom väčším ako 90° a dokonca sa takmer presne odrážali späť! Geiger a Marsden to opakovane testovali pomocou mierne odlišných experimentálnych nastavení predtým, ako to oznámili Rutherfordovi. Takýto výsledok nikto nečakal.
Rutherford opakovane pripomenul, že bol týmto výsledkom mimoriadne ohromený. Počas jednej zo svojich prednášok na univerzite v Cambridge vyslovil slávne slová, ktorých drámu žiadny preklad nedokáže vyjadriť:
Bola to celkom neuveriteľná udalosť, aká sa mi v živote stala. Bolo to takmer také neuveriteľné, ako keby ste vystrelili 15-palcovú strelu na kúsok hodvábneho papiera a ten sa vrátil a zasiahol vás.
Ernest Rutherford
Pokračovanie vyššie uvedeného citátu je prezrádzajúce: „Po krátkom premýšľaní som dospel k záveru, že rozptyl pod týmto uhlom bol pravdepodobne výsledkom jedinej kolízie. Urobil som zodpovedajúce výpočty; presvedčili ma, že je možné len jedno vysvetlenie: atóm je systém, ktorého prakticky celá hmota je sústredená v mikroskopickom jadre, kladne nabitá.“
Tu je záver hodný fyzika: keď dobre vykonaný experiment nesúhlasí s predchádzajúcimi presvedčeniami alebo dokonca zavedenou teóriou, zahodíme presvedčenia a prepracujeme teóriu.
Rutherfordov výklad
Použime tri diagramy zobrazené na obrázkoch 5, 6 a 7, aby sme videli, čo Rutherford videl vo vnútri atómu. Vo všetkých diagramoch sa častica α s energiou 1 MeV (to zodpovedá rýchlosti takmer 7000 km/s) približuje k atómu centrálne - kolízny parameter je rovný nule. Predpokladáme, že náboj jadra atómu sa rovná náboju zlatého jadra - 79 elementárnych nábojov.Sila elektrostatického odpudzovania jadra je opačná ako rýchlosť častice α.
Predpokladáme, že atóm zostáva nehybný a pýtame sa, či Coulombova sila dokáže zastaviť časticu α a poslať ju späť predtým, ako prejde stredom jadra. Ak áno, potom častica α bude urýchlená Coulombovou silou a vráti sa tam, odkiaľ prišla, a jej uhol rozptylu bude 180°. Ak nie, potom na druhej strane častica α poletí ďalej a uhol rozptylu sa bude rovnať nule. Ukazuje sa, že tu je rozhodujúca veľkosť atómového jadra.
Rj=0,1 Å, t.j. jadro je 10x menšie ako atóm
Obrázok 5 ukazuje situáciu v mierke celého atómu, ktorého polomer je 1 Å. Polomer jadra je Rj=0,1 Å. Horný graf ukazuje závislosť Coulombovej sily od vzdialenosti od stredu jadra. Táto sila dosahuje maximálnu hodnotu tesne pod 0,4 mN, keď častica α vstúpi do jadra. Od tohto bodu sa Coulombova sila lineárne znižuje a v strede jadra dosahuje nulu.
Závislosť rýchlosti častice α na rovnakej vzdialenosti je nakreslená v spodnej časti diagramu. Táto rýchlosť klesá s približovaním sa k okraju jadra. Po vstupe do oblasti jadra je tento pokles menej výrazný – to zodpovedá poklesu hodnoty Coulombovej sily. Celkovo sa rýchlosť znížila o necelé 2 %. Po prechode stredom jadra sa α-častica zrýchli, čím opustí jadro a následne celý atóm.
Záver: Prítomnosť α-častíc s energiami rádovo 1 MeV a vyššími (také používali Geiger a Marsden), odrazených späť, vylučuje takú veľkú veľkosť jadra – rádovo 0,1 Å.
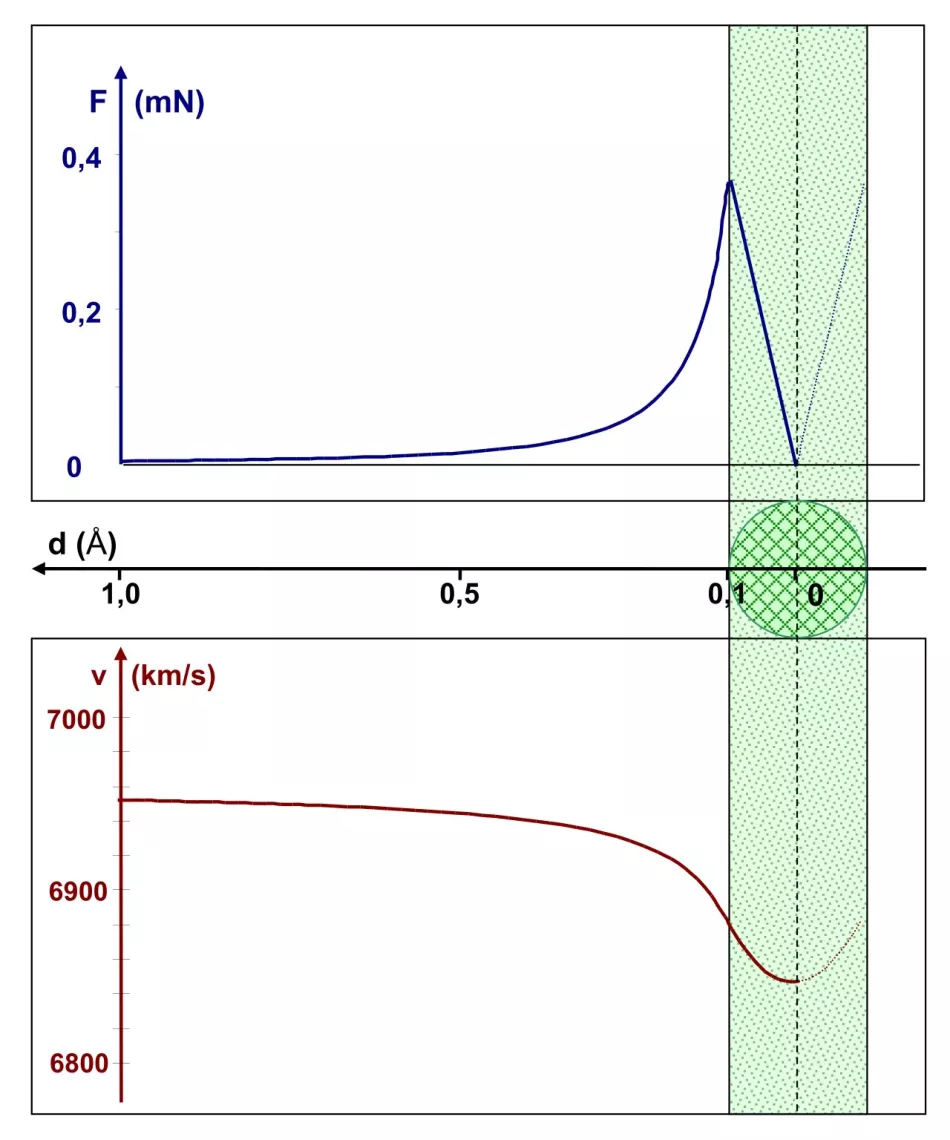 Ryža. Obr. 5. Grafy Coulombovej sily a rýchlosti častice α ako funkcia vzdialenosti d od stredu atómového jadra Obr.
Ryža. Obr. 5. Grafy Coulombovej sily a rýchlosti častice α ako funkcia vzdialenosti d od stredu atómového jadra Obr.
Vodorovná os spoločná pre oba grafy sa nachádza medzi nimi. Jadro s polomerom 0,1 Å (zobrazené zelenou farbou) sa nachádza na pravej strane grafu, takže os vzdialenosti má nezvyčajné zatočenie: doľava.
Rj=0,01 Å, t.j. jadro je 100-krát menšie ako atóm
Preto v ďalšom kole výpočtov zmenšíme polomer jadra desaťkrát, na 0,01 Å. Obrázok 6 ukazuje túto situáciu, aj keď už neobsahuje atóm, ktorého približný polomer je 1 Á. Všimnite si mierku na osi vzdialenosti - graf teraz pokrýva oblasť od 0,1 Å do stredu jadra. Jeho priebeh je veľmi podobný predchádzajúcemu. Rozdiel spočíva v mierke. Coulombova sila dosahuje na okraji menšieho jadra 40 mN, čo je stokrát viac ako u väčšieho jadra. Je to pochopiteľné: pomer polomerov 1:10 znamená pomer síl 100:1. To vedie k zníženiu rýchlosti častíc α asi o 18 %. Neklesá však k nule, takže častica alfa prejde stredom jadra a preletí atómom.
Záver: atómové jadro musí mať polomer dokonca menší ako 0,01 Å, inak neodrazí α-častice späť.
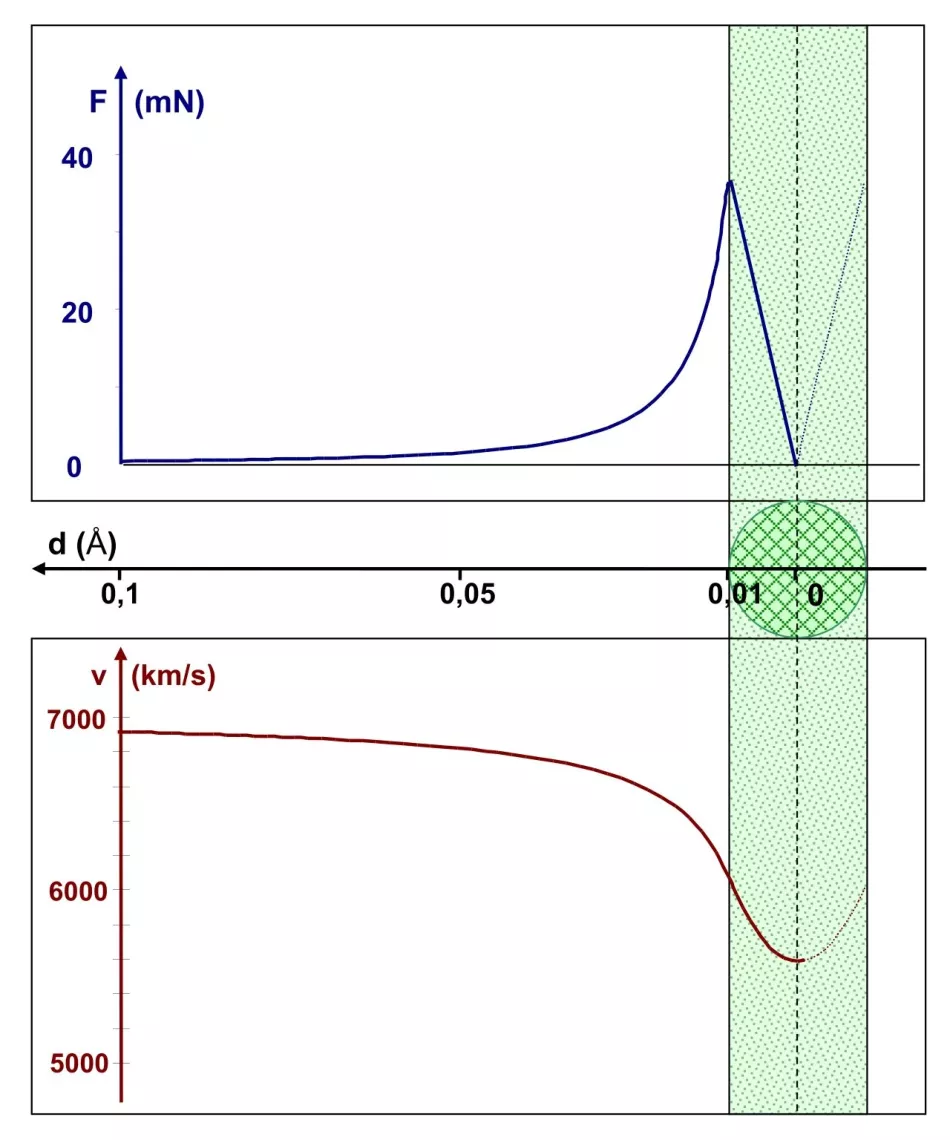 Ryža. 6. Grafy závislosti Coulombovej sily a rýchlosti častice α v závislosti od vzdialenosti d od stredu atómového jadra s polomerom 0,01 Å Obr.
Ryža. 6. Grafy závislosti Coulombovej sily a rýchlosti častice α v závislosti od vzdialenosti d od stredu atómového jadra s polomerom 0,01 Å Obr.
Maximálna hodnota sily je stokrát väčšia ako v prípade znázornenom na obrázku 5, čo má za následok väčší pokles rýchlosti častice α.
Rj=0,001 Å, t.j. jadro je 1000-krát menšie ako atóm
Znova znížme polomer jadra desaťkrát - na jednu tisícinu angstromu - bez zmeny ostatných parametrov. V rýchlostnom diagrame si všimneme (obr. 7.) novinku: jej hodnota klesne na nulu, keď je častica α vo vzdialenosti asi 0,0023 Å od stredu jadra, t.j. 0,0013 Å od jeho okraja. V tejto polohe bola α-častica urýchlená v smere, z ktorého prišla – jej uhol rozptylu je 180°. Stojí za zmienku, že Coulombova sila dosiahla hodnotu asi 700 mN.
Záver: atómové jadro s polomerom 0,001 Å je schopné zastaviť α-časticu s energiou 1 MeV a rozptýliť ju späť. Existuje na to dokonca určitá „okraj“, keďže častica sa zastaví o niečo viac ako 0,001 Å od okraja takého jadra.
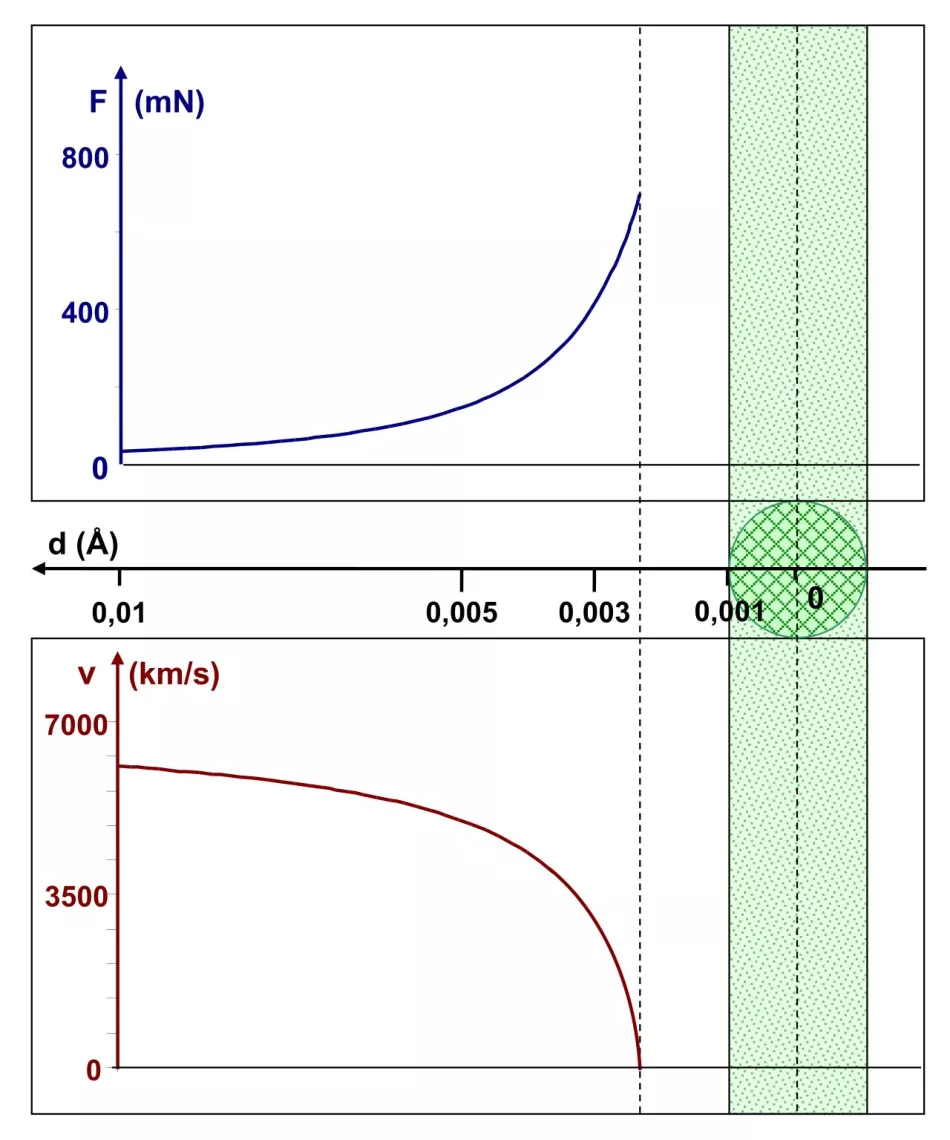 Ryža. 7. Grafy závislosti Coulombovej sily a rýchlosti častice α v závislosti od vzdialenosti d od stredu atómového jadra s polomerom 0,001 Å Obr.
Ryža. 7. Grafy závislosti Coulombovej sily a rýchlosti častice α v závislosti od vzdialenosti d od stredu atómového jadra s polomerom 0,001 Å Obr.
Vo vzdialenosti asi 0,0013 Å od okraja sa častica alfa zastaví a zrýchli v smere odkiaľ prišla.
Záver
Prítomnosť α-častíc s energiou 1 MeV, rozptýlených späť, vylučuje polomer atómového jadra väčší ako 0,002 Å. Geiger a Marsden vyrobili alfa častice s energiami v rozmedzí od 1 MeV do približne 5 MeV z niekoľkých rôznych rádioaktívnych prípravkov. Všetci boli hodení späť. Podobné úvahy a výpočty umožnili Rutherfordovi určiť maximálny možný polomer atómového jadra, ktorý je približne 0,001 Å.
Ďalšie štúdie štruktúry atómu pomocou rôznych častíc, vrátane protónov urýchľovaných v urýchľovačoch na stále vyššie energie, umožnili skúmať veľkosti jadier rôznych atómov. Ukázalo sa, že polomer jadra sa zväčšuje s rastom jeho hmotnostného čísla A, ale nedosahuje 0,0001 Å alebo 10-14 m.
Paralelné štúdie atómového zloženia umožnili približne štvrťstoročie po experimentoch uskutočnených pod vedením Rutherforda a po objavení neutrónu v roku 1932 určiť zloženie atómových jadier rôzne prvky a ich izotopy.